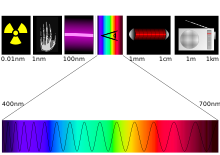
 (400-800 нм) и ближнего инфракраснонго (0,8 – 1,5 мкм).
(400-800 нм) и ближнего инфракраснонго (0,8 – 1,5 мкм).Исследования химического действия излучения на различные вещества и попытки его теоретического истолкования начинаются с конца XVIII в., когда Дж. Сенеби высказал предположение о том, что необходимая для достижения определённого химического эффекта продолжительность действия света обратно пропорциональна его интенсивности. В 19 в. параллельно происходило открытие новых реакций органических и неорганических веществ под действием света и физические и химические исследование механизма и природы фотохмическихой реакции. В 1818 Т. Гроттус отверг гипотезу о тепловом действии света, предположил аналогию в воздействии на вещество света и электричества и сформулировал принцип, согласно которому причиной хмического действия может 6ыть только тот свет, который поглощается веществом (закон Гротгуса). Дальнейшими исследованиями было установлено, что количество продукта фотохмическихой реакции пропорционально произведению интенсивности излучения на время его действия (Р. Бунзен и Г. Роско, 1862) и что необходимо учитывать интенсивность только поглощенного, а не всего падающего на вещество излучения (Я. Вант-Гофф, 1904). Одно из важнейших достижений фотохимии - изобретение фотографии (1839), основанной на фотохмическихом разложении галогенидов серебра.
Принципиально новый этап в развитии фотохимии начался в 20 в. и связан с появлением квантовой теории и развитием спектроскопии. А. Эйнштейн (1912) сформулировал закон квантовой эквивалентности, согласно которому каждый поглощенный веществом фотон вызывает первичное изменение (возбуждение, ионизацию) одной молекулы или атома. Вследствие конкуренции хмических реакций возбужденных молекул и процессов их дезактивации, а также обратного превращения нестабильных первичных продуктов в исходное вещество, хмического превращения претерпевает, как правило, лишь некоторая доля возбужденных молекул. Отношение числа претерпевших превращение молекул к числу поглощенных фотонов называется квантовым выходом фотохмическихой реакции. Квантовый выход, как правило, меньше единицы; однако в случае, напр., цепных реакций он может во много раз (даже на несколько порядков) превышать единицу.
В России важное значение имели в начале ХХ в. работы П.П. Лазарева в области фотохимии красителей и кинетики фотохмических реакций. В 40-е гг. А.Н. Терениным была высказана гипотеза о триплетной природе фосфоресцентного состояния, играющего важную роль в фотохмических реакциях, и открыто явление триплет-триплетного переноса энергии, составляющее основу одного из механизмов фотосенсибилизации хмических реакций.
Использование достижений квантовой химии, спектроскопии, хмической кинетики, а также появление новых экспериментальных методов исследования, в первую очередь методов изучения очень быстрых (до 10"12 с) процессов и короткоживущих промежуточных веществ, позволило развить детальные представления о законах взаимодействия фотонов с атомами и молекулами, природе возбужденных электронных состояний молекул, механизмах фотофизические и фотохмических процессов. Фотохмические реакции протекают, как правило, из возбужденных электронных состояний молекул, образующихся при поглощении фотона молекулой, находящейся в основном (стабильном) электронном состоянии. Если интенсивность света очень велика [более 10м фотонов/ (с-см2)], то путем поглощения двух или более фотонов могут заселяться высшие возбужденные электронные состояния и наблюдаются двух- и многофотонные фотохмические реакции (Двухквантовые реакции, Многофотонные процессы). Возбужденные состояния не являются лишь "горячей” модификацией их основного состояния, несущей избыточную энергию, а отличаются от основного состояния электронной структурой, геометрией, химической свойствами. Поэтому при возбуждении молекул происходят не только количественные, но и качеств, изменения их химической поведения. Первичные продукты реакций возбужденных молекул (ионы, радикалы, изомеры и т.п.) чаще всего являются нестабильными и превращаются в конечные продукты в результате серии обычных термических химических реакций.
Для качеств, и количеств, исследования продуктов используют всевозможные аналитические методы, в т. ч. оптической спектроскопию и радиоспектроскопию. Для определения дозы облучения и квантовых выходов применяют актинометрию. Свойства короткоживущих возбужденных состояний обычно изучают методами оптической эмиссионной (флуоресцентной и фосфоресцентной) и абсорбционной спектроскопии. Особенно важное значение для исследования механизмов фотохмических реакций имеют импульсные методы: импульсный фотолиз, лазерная спектроскопия и др. (см. Люминесцентный анализ). Эти методы позволяют изучать кинетику первичных реакций возбужденных молекул, нестабильные промежут. продукты и кинетику их превращений. Фотохмические методы применяют и для исследования обычных термических реакций радикалов, ионов и др. промежуточных веществ. Важную информацию о механизмах фотохимии дают радиоспекототроскопические методы, основанные на динамичной поляризации ядер и электронов (Химическая поляризация ядер).
В современной выделяют следующие разделы: фотохимия малых молекул, позволяющую выяснить динамику элементарного акта в возбужденных электронных состояниях молекул; органических и неорганических Фотохимию, изучающие фотопревращения соответствующих хмических соединений и методы фотохмического синтеза; механистичную (физическую) фотохимию, изучающую механизмы и кинетические закономерности фотохмических реакций и тесно связанная с фотофизикой, химической кинетикой, квантовой химией, теорией строения молекул и др. разделами физические химии.
Важные практические применения фотохимии связаны с фотографией, фотолитографией и др. процессами записи и обработки информации, промышленном и лабараторным синтезом органических и неорганических веществ (фото-нитрозирование циклогексана с целью получения капролакототама, синтез витаминов группы D, напряженных полициклич. структур и др.), синтезом и модификацией полимерных материалов (фотополимеризация, фотомодификация и фотодеструкция полимеров), квантовой электроникой (фотохмических лазеры, затворы, модуляторы), микроэлектроникой (фоторезисты), преобразованием солнечной энергии в химическую.
Фотохмических процессы играют очень важную роль в природе. Биол. фотосинтез обеспечивает существование жизни на Земле. Подавляющую часть информации об окружающем мире человек и большинство животных получают посредством зрения, основанного на фотоизомеризации родопсина, которая запускает цепь ферментативных процессов усиления сигнала и тем самым обеспечивает чрезвычайно высокую чувствительность вплоть до регистрации отдельных фотонов. Озон образуется в верх. слоях атмосферы из кислорода под действием коротковолнового (<180 нм) излучения Солнца по реакции:
O2 + hv = O + O O3
Он поглощает излучение Солнца в области 200-300 нм, губительно действующее на живые организмы.
